1. exploration (외삽, 동물실험결과를 사람에게 어떻게 적용할것인가?)
- 어떤 물질도 독성을 나타낼수 있으며 노출되는 경로에 따라 독성이 달라질수 있다.
- 신약을 개발할때 안정성을 검사하는것이 매우 중요하다 하지만 모든 위험을 다 대비하기는 어렵다
- 동물실험결과를 사람에게 직접적용하기 어렵다.
-90년대 초반 magin johnson hiv감염, 프레디 머큐리 사망등이 알려지면서 수십억 달러의 연구비가 동물실험에 사용되었다.
하지만 hiv 감염과 질병이 동물실험에서는 재현이 잘 되지 못함을 알지 못하여서 큰 결과를 얻지 못함
= exploration의 개념을 잘못이해한것의 예
2. 반수치사랑(lethal50, LD50)
- LD50의 의미, 구하는 방법
- LD50의 장점, 한계
- 일반독성시험, 특수독성시험 구분
- 급성독성시험, 아급성독성시험, 만성독성시험 구분
- 치료지수 TI 의 의미
- 독성시험에서 있어 dose-response 시험의 중요성
- 독성시험은 인체에 적용할 수 있는 시험법을 사용
= 인체에 응용할 수 있는 적절한 방법 (동물 마다 독성이 다름)
- 고용량실험으로 저용량 위험성 평가
=용인 될수 없는 독성이지만 표본수가 적은 동물실험으로 검증할 수 없다는 문제가 발생
- 어떤 물질의 안정성을 입증하는 것보다 독성을 특정 짓는것이 중요하다
= 물질이 어떠한 독성도 없다는 것을 증명하기는 어렵다.
- NOAEL
= no-observed adverse effect level=독작용을 일으키지 않는 최대 용량
- LOAEL
= lowest-observed adverse effect level=독작용이 관찰되는 최소 용량
- ADI
=accetable daily intake = 주로 식품첨가물, 만성노출에 대한 허용치를 결정하는 출발
3. Xenobiotics (외래물질)
- Xenobiotics의 의미와 특성 (크기, 성질, 용해성, 활성, 독성기전 )
= 외부에서 들어오는 약물, 환경오염물질 등 인체 내에서 생성되지 않으면서 정상적인 식이에 포함되지 않는 모든 물질
= 인체 내로 들어오는 독성물질의 종류, 물리화학적 성질
= ADME
= target organ
= toxic mechanism에 대한 정보
- 독성이 없던 xenobiotics가 체내에서 독성이 생기는 이유
= 독성물질은 비활성상태로 체내에 들어온 후에 활성이 있는 형태로 바뀌기 위해
자연분해 (natural decomposition) 되거나, 효소 에 의해 전환 (biotransformation) 됨
- Xenobiotics 인체 내로 들어오기 위해 많은 막을 건너야한다.

=Lipophilic한 독성물질이 체내로 들어와서는(체외에서는 반응성이 없어야되니까)
hydrophilic하게 생체전환되어 배출(체내에서는 반응성이 많아야되니까)
- Xenobiotics가 독성을 나타내기 위해 상호작용하는 생체 내 거대분자
= 내인성물질들은 생체 내 거대분자와 '비공유 결합'을 하게됨 = 쉽게 결합하고 분리되어 생물분자의 가역반응과 재활용성 확보
( 내인성물질 = 단백질, 당, 지질성분을 바탕으로 해서 분자량이 크고, 호르몬, 사이토카인 같이 세포 밖에서 막수용체에 신호를 전달, 스테로이드 같이 세포막을 투과하는 경우 크기가 비교적 작음)
= 외인성물질들은 공유결합을 해서 상호작용을 함 = 결합하면 잘 불리되지 않는 비가역반응을 통해 독성 유발
(외인성물질은 크기가 크면 세포막 투과가 어려워 1 kdalton 이하 참고, 1d=수소1g/mole
아미노산 1개는 평균 110dalton이므로 아미노산 50개로 구성된 단백질은 5500dalton
올리고 뉴클레오타이드는 330dalton 1개의 아미노산은 3개의 염기로 구성되므로 50*3*330=50kd)
- Xenobiotics가 독성을 나타내기 위해 생체 내 거대분자와 어 떤 상호작
- 일급발암물질을 약으로 사용하고 있는 이유
=IARC(international agency for research on cancer)의 그룹1 발암물질이 약으로 사용됨
예) 에스트로겐은 1급 발암물질이지만 약으로 쓰이는 이유는 해결방법을 알고 있음
일반적으로 크기는 (1 kd )이하이다.
특성은( 유기 )화합물이다.
용해성은 ( 지용 )성 이다. (비활성)상.태로체내에들어온다.
체내에서 ( 생체전환)된 후 배설되거나 독성을 나타낸다.
체내의 거대분자와 (비가역)적 상호작용을 통 해 독성을 나타낸다.
4. 생체대사 (biotransformation) : 외인성물질이 몸 속에 들어와서 생체전환되는 과정
(개요)
외인성물질은 제1상반응에 의해 극성 (polar)을 갖게 됨.
극성은 제2상 반응이 일어나기 위해 필요
극성은 전자를 끌어당기는 힘
전하분포가불균일할 때 발생
산소와 수소가 결합할 때 산소의 원자핵이 전자를 끌어당겨 부분적으로 음전하를 띠게 되고, 수소는 부분적으로 양전하를 띠게됨
일반적으로 xenobiotics는 polar하지 않음
Phase 1 반응에 의해 polar group이 노출되거나 도입
Polar group이 있으면 Phase 2에 의해 conjugation되어 배출
Polar group이 macromolecule을 공격.
결론적으로 hyrophilic하게 만들어 배출하기 위해 polarity를 부여한 결과 독성이 유발됨
Lipophilic한 독성물질이 체내로 들어와서는 hydrophilic하게 생체전환되어 배출
결국 체내에 들어온 외인성 물질을 배출하기 위해 생체전환 시킨 결과,
비활성이던 물질이 활성을 가지게 되어 거대분자와 상호작용하여 독성을 유발하게 된다.
Xenobiotic의 90% 이상 간에서 대사
- Biotransformation의 단계
Phase I and II reaction
제1상 반응
Xenobiotics가 산화 (oxidation), 환원(reduction) , 가수분해 (hydroxylation) 의해 극성 (polar)을 갖게 된다.
-OH, -COOH, -SH, -O- or –NH2 등의 작용기도입
Cytochrome P450 (P450) 약 80-90% 처리 Flavin-containing monoxygenase (FMO)등
제2상 반응
Xenobiotics의 극성부위에 sulfate,glucuronide, glutathion등이 포합 (conjugation) 된다.
UDP-glucuronosyltransferase (UGT) 30% Sulfotransferase (SULT) N-acetyltransferase (NAT) Methyltransferase (MT) Gutathione-S-transferase (GST)
제1상 반응에 관여하는 효소 (CYP450)와 제 2상반응에 관여하는 효소의 세포 내 localization은 Microsome (SER) Cytosol
이유 : 지질에 대한 용해성이 높은 외인성물질은 주 로 microsome에서 대사됨
Phase I Cytochrome P450 Microsome
Phase II enzyme Cytosol, microsome, mitochondria
고용량으로 동물실험해서 저용량 노출에 의한 독성을 평가 = 에임즈 테스트
<정리>
Xenobiotics이 극성, 친수성으로 전환되어 bioinactivation
친전자성 (electrophilic) 물질=전자부족로 전환되어 네 가 지 거대분자의 친핵성 (nucleophile)부위=전자풍부 를 공격
친전자성 대사체는 전자가 부족한 활성중간대사물질을 의미
친전자성 대사체는 GSH conjugation에 의해 친 수성으로 전환되어 배출


< Phase I reaction (Cytochrome P450 dependent) >
- Cytochrome P450에서 P는 색소, 450 (nm)은 최 대흡광도를 나타냄, P450의 분류는 효소의 염기서열 또는 아미노산 서열의 동일성을 기준
- 사람의 P450 유전자는 57개인 반면 동 물의 P450 유전자는 101개
동물이 인간보다 P450 유전자를 더 많 이 가지고 있는 이유는 동물이 P450의 기질이 되는 다양한 외인성 물질을 포함하고 있는 더 많은 종류의 식물 성 먹이를 취하기 때문일 것으로 추정 ( 면접 : 몸에 좋은 샐러드를 개나 고양이에게 먹인 다면?)
- 독성물질에 대한 P450의 유전자의 종류, 발현조절, 및 기능에 차이 (사람과 동물 또 는 동물과 동물 상호간의 차이)가 있음
=> 이러한 차이는 독성물질에 대해 종에 따라 감수성이 달라지는 주요 요인
=>동물실험에서 얻은 결과를 인간에게 외삽 (extrapolation)하는데 어려움이 있는 약물대사효소의 유전자가 많이 다르니 독 성실험결과도 다르기때문
- 11 channels in P450 : 채널의 다양성과 유연성으로 인해 P450의 광 범위한 기질을 촉매할 수 있는 기전으로 추정
- 일반적인 효소와 약물대사효소의 기질 특이성의 차이는 약물대사효소는 일반적인 효소보다 기질특이성이 낮다는것
= 약물대사효소는 일반적인 효소와 달리 외부 에서 무수히 많은 종류의 화합물에 대하여 일 일이 다른 약물대사효소를 이용하여 대사시 키는 것이 불가능하므로 기질특이성을 낮추 어 다양한 기질을 촉매 (약물대사효소는 특이적인 생성물을 만들지 않고 다만 수 용성을 증가시키면 되기 때문)
- P450의 분포 조직, 세포 그리고 세포 내 소기관
: P450은 대부분 간에만 있어야 할 것 같지만 신장, 폐, 부신, 생식선, 뇌 등 다양한 조직에서 발현
: P450은 xenobiotics의 대사뿐만 아니라 생리 활성물질의 동화작용에도 관여하기 때문에 기관, 조직과 세포 등에 특이적으로 분포
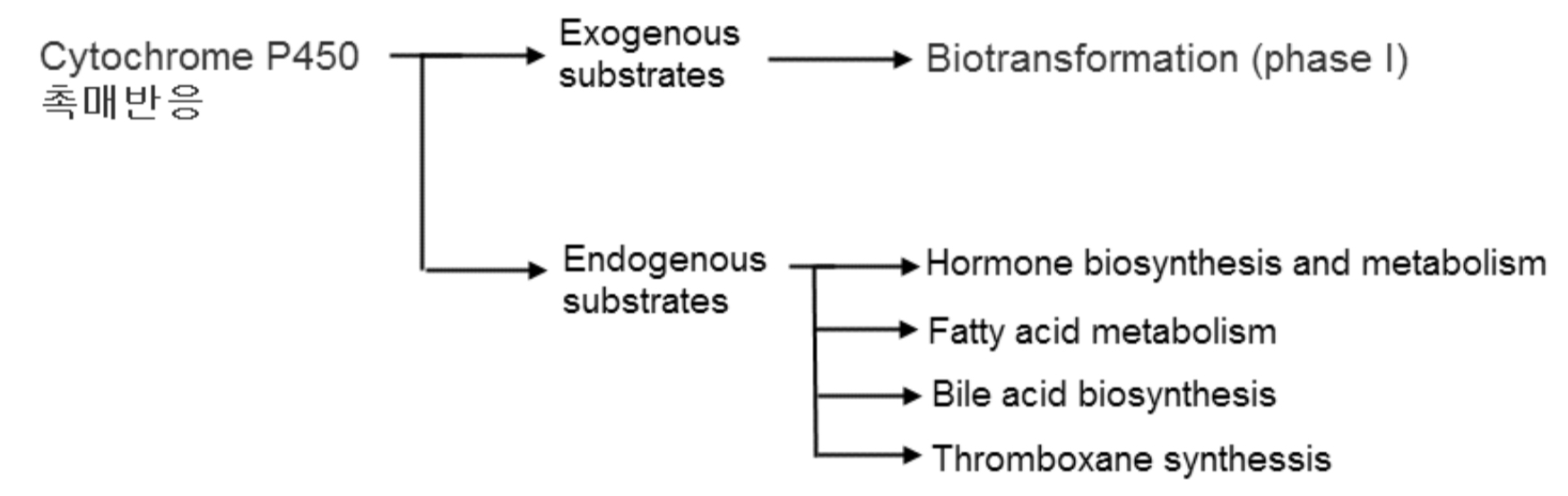
- P450의 주요기능
외인성물질의 생체전환뿐 아니라 P450은 생체의 항상성 유지에 대한 기능으로는 호르몬 합성과 대사, 지방산 대사, 담즙산 합성 그리고 thromboxane 합성 등 중요한 역할 = P450은 외인성물질뿐 아니라 내인성물질 대사에도 관여함
[촉매반응]
1) Hydroxylation은 P450에 의한 대표적 인 촉매반응이다.
hydrogen abstraction, oxygen rebound

2) Epoxidation은 xenobiotics의 독성을 유발하는 중요한 biotransformation 이다.

- Xenobiotics를 대사시키는 P450는 대부분 간 (70%)의 소포체에 존재
Microsomal membrane (80%): xenobiotics biotransformation
Innermitochondrial membrane. (20%): steroid, vitD3 biosynthesis
- Catalytic cycles of cytochrome P450

P450은 기질에 산소원자를 첨가하며 이에 필 요한 전자를 NADPH로 부터 얻음
- p450 효소특징
P450는 xenobiotics뿐 아니라 endogous substrate의 대사에도 관여하여 생명체의 항상성을 조절하므로 유도효소이면서 구성 효소의 특성을 함께가짐
- P450s in extrahepatic tissues (소장)
소장상피 =CYP3A4 (70%), CYP2C9(15%)
CYP3A4는 first-pass metabolism에 매우 중요 한 역할을 수행한다.
예)
장기이식 후 면역억제에 사용되는 cyclosporin은 CYP3A4에 의해 대사된다.
자몽 중의 어떤 성분은 CYP3A4의 활성을 억제한다.
하루 한 개의 자몽 섭취로 cyclosporin의 혈중 농도를수배올릴수있다.
부작용으로신독 성이 나올 수 있다.
- P450s in extrahepatic tissues (폐와 호흡기)
폐로 들어오는 xenobiotics를 대사시키기 위함
-그외 kidney, skin, brain등에서 발견
< Phase II (제2상 반응)에 의한 생체전환 >
: 제 2상 반응은 제1상 반응 후 생성된 극 성대사체 및 친전자성대사체 등 모든 대 사체의 체외배출을 위해 친수성으로 전환 시키는 포합반응

1) Glucuronic acid conjugation : 가장 대표적

2) Sulfate conjugation : SO3- 를 –OH, -NH2에 포합

3) Acetylation conjugation : Acetyl-CoA로부터 기질의 아세틸화

아세틸화 포합반 응은 N-acetyltransferase이Acetyl-CoA로부터 분리된 acetyl group 이 기질 전이에 전이되어 이루어짐
CoAS-COCH3: Acetyl-CoA. 다른 포합반응에 비해 친수성이 낮아 체외배출에 효율적이지 않다.
4. Methylation

Methionine으로부터 메 틸기(CH3) 공여체인 Sadenosylmethione (SAM)이 합성되어 methyltransferase에 의해 외인성물질 HX-R에 메틸기가 전달된다. Ad: adenine. 다른 포합반응에 비해 친수성이 낮다. 오히려 친지질성을 높 여 독성을 증가시키는 경우도 있다.
5. Amino acid conjugation : 대표적인 포합아미노산인 glycine과 glutamate

6) GSH conjugation
(면접)
다른 포합반응과 달리 제1상반응에서 생 성된 친전자성대사체의 포합을 유도하는 유일한 방법이라는 것이다. 외인성물질 노출에 의해 발생하는 독성 의 무독화를 유도하는 가장 중요한 기전
GSH 포합반응은 광범위한 기질특이성을 가 진 GST에 의해 수행된다. 대부분 세포질에 존재한다. 전체 세포질 단백질 중 3-5%를 차지한다. Electrophile을 포합시키는 유일한 효소이며, 매우 많은 양이 세포 내에 존재하여 해독작용 에 중요한 역할을 수행한다

글루타치온 : GSH(glutathione 또는 γ- glutamylcysteinyl glycine)은 3개 아미노산인 glutamate, cysteine 과 glycine으로 구성되어 있으며 cysteine의 SH가 포합반응에 있 어서 중요한 전자공여체
GSH는 세포질에 약 90% 미토콘드리아에 약 10%, 그 외 소량이 소포체에 존재한다. 성인체내에 1-10 mM,농도로 가장 많이 존재하 는 비단백질 thiol함유 유기황화합물
(면접) 유기라디칼대사체의 연쇄반응을 통해 생성된 수많은 라디칼이 마치 싱크대에서 오물을 청소하듯이 GSH를 비롯하여 SOD(superoxide dismutase)에 의해 청소되는 현상을 Radical sink hypothesis

GSH로 환원 : GSSG는 NADPH를 조효소로 하여 GSH reductase,에 의해 정상적인 생리적 조건하에서 GSH의 형태로 약 98% 정도 환원된다. 나머지 GSSG는 단백질의 SH와 결합한 형태인 혼합형 disulfide, 또는 GSSG자체로 존재한다. 산화적 스트레스가 심한 경우 GSH로 환원할 수 있는 세 포의 능력한계로 GSH가 고갈
고갈상황 : 산화적 스트레스가 심한 경우 GSH로 환원할 수 있는 세포의 능력한계로 GSH가 고갈될 수 있다. GSH는 세포질에 약 90% 미토콘드리아에 약10% 존재한다. 미토콘드리아에서 ROS를 과잉 생산하 면, GSH가 고갈될 수 있다. GSH가 고갈되면 ROS에 의한 미토콘드리아 손상 이 유발될 수 있다
Xenobiotics 대사로 인해 electrophile이 많이 생 성되는 경우 GSH가 고갈될 수 있다. GSH가 고갈되면 electrophile에 의한 손상이 유 발될 수 있다.
예) 타이레놀 독성

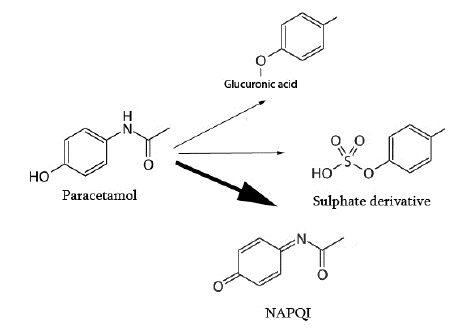
타이레놀 Acetaminophen, (N-acetyl p-amino phenol) 은 극성부위 (OH)가 있어 sulfate 또는 glucuronide conjugation에 의해 수용성이 증가되어 배설된다

타이레놀의 섭취가 많아 지면, CYP2E1등에 의해 독성대사체 (electrophile) 가 생성된다.
생성된 electrophile은 GSH conjugation된다. <nontoxic>

독성대사체 (electrophile) 가 과잉생성되면 GSH가 고갈된다. Electrophile은 macromolecule의 nucleophile을 공격하여 비가역적 독성을 유발한 다. <Cell death>
- 고양이 : 고양이게는 500mg 한 알 분량도 웬만한 체중까지는 치사량에 해당한다. 그 이유는 고양이는 거의 육식을 하기 때문에 식물에서 나오는 화합물을 대사하는 능력 중 하나인 글루쿠론산 포합과정이 진화단계에서 소실되었다. 따라서 아세트아미노펜에 대해서 다른 동물에 비해 더 큰 독성 반응을 나타낸다. 아세트아미노펜 뿐만 아니라 모든 약물은 대사하는 속도나 효율이 동물에 따라 다르므로 사람에게 처방하는 약을 함부로 동물에 먹여서는 안된다.


-Acetaminophen 뿐만 아니라 대부분의 동물약이 개, 고양이, 소, 말, 돼지 등 축종에 따라 투약 용량과 그 에 따른 부작용도 다르게 나타남
- Acetaminophen은 개(Canine)에 있어 10~15mg/kg q8h PO, 송아지(Calves)는 50mg/kg로 시작해 이후에 30mg/kg PO q6h로 투약한다.
- Acetaminophen제제는 고양이에게는 투약금기의약품에 해당
- Acetaminophen의 해독은 대부분 Glucuronidation/sulfation을 통해 소변으로 배출되며 일부만 CYP450에 의해 독성물질인 NAPQI로 대사되고 이는 간의 Glutathione포합에 의해 해독
- 고양이는 Glucuronidation에 관여하는 glucuronyl transferase의 활성이 사람이나 개보다도 1/10정도로 낮기 때문에 대부분의 타이레놀이 CYP에 의해 NAPQI로 전환되고 이어 glutathione포합 반응이 일어나는데 문제는 glutathione의 빠른 고갈이다.
- Glutathione을 너무 많이 소모해 간, 적혈구에 서 모두 고갈되면 간세포와 적혈구가 파괴되고 이어 메트헤모글로빈혈증, Heinz body 빈혈, 간수치상승 등으로 사망에 이르기도 한다.
- 해독제로는 약국에서 흔히 사용되는 N-acetylcystein(객담용해제), 비타민C, 시메티딘 등이 있다.
- N-acetylcystein은 간의 글루타치온을 복구하고 간 혈행개선, 자유라디칼을 제거하는 역할을 하며, 비타민C는 비정상적인 헤모글로빈을 줄이는 데 도움을 주고, 위장약으로 처방되는 시메티딘은 CYP억제제로서 Acetaminophen의 NAPQI로의 전환을 늦추기 위해 사용된다.
(참고) 시메디틴

< 동물실험기법 Animal Experiment >

- Germ free animal: 검출 가능한 미생물이 없는 동물 심지어는 장 내에서 소화를 돕는 미생물도 없다.
germ free animal을 얻기 위해서는 무균 시설에서 모체로부터 제왕절개술이나 자궁적출을 해야 한다.
- Gnotobiotic animal: 감염된 미생물이 명확한 동물. 그러기 위해서는 germ free animal에 명확하게 분리된 미생물을 정착시켜야 한다.
- SPF(specific pathogen-free) animal: 감염되지 않은 미생물이 명확한 동물. 즉, 특정 병원성 박테리아나 바이러스에 감염되지 않았다고 명확히 말할 수 있는 동물
- Conventional animal: 일반적으로 보는 가축이나 애완동물, 야생 동물 감염된 미생물과 감염되지 않은 미생물이 불명확 하다
< 시료 및 약제의 투여법 >
- 피하주사(Subcutaneous Injection)
- 복강내주사(Intraperitoneal Injection)
- 근육내 주사(Intramuscular Injection)
- 피내주사(Dermal Injection)
- 뇌내주사(Intracerebral Injection)
- 정맥내 주사(Intravenous Injection)
--설하정맥 주사(Injection into the Sublingual Vein)
-- 음경정맥내 주사(Injection into the Penile Vein)
-- 꼬리정맥내 주사(Injection into the Caudal Vein)
-- 뒷발허리 정맥내 주사 (Injection into the Dorsal Metatarsal Vein)
- 경구투여(Oral Administration)
< 형질전환실험동물 Transgenic animal >
< 실험동물의 복지 및 윤리 Experimental Ethics >
- Good Care and Good Science go Hand in Hand
-외국 실험동물 복지정책의 특징
(미국, 독일, 네덜란드, 영국, 프랑스, 스웨덴, 일본 등의 경우)
1. 실험동물의 관리와 사용에 관한 지침에 실험동물 복지 규정을 명시함.
2. 과학자와 시민 등 다양한 분야의 사람들로 구성된 위원회를 설치하여 연구내용에 적합한 동물실험의 수행과 동물복지의 준수 여부를 항시 감시하는 제도적 장치를 마련함.
3. 실험동물의 복지에 관련한 내용을 실험방법 별로 구체적으로 기술하여 위반 여부를 명확하게 판단할 수 있도록 함.
4. 동물실험에 종사하는 실험자가 충분한 교육을 받은 후 동물실험에 임할 수 있도록 제도화하고, 위반한 실험자는 엄격한 처벌을 받도록 함.
5. 실험동물 복지에 관한 규정이 과학적 실험결과를 도출하는데 방해 혹은 지장을 초래하지 않도록 규정의 수정과 제도적 보안을 유연하게 함.
-국내의 실험동물 복지정책
1. 농림부의 동물보호법 제3조에 “과학적 목적으로 사용되는 동물에게는 가능한 한 고통을 주지 말아야 한다”는 내용이 기술되어 있음.
2. 정부차원에서의 실험동물의 사용과 관리에 관한 규정이 없으므로, 각 연구 기관별로 획일화되지 않은 개별적 규정이 만들어져 혼란을 야기할 수 있음. 그러므로 정부의 담당부처가 실험동물의 관리와 복지에 관한 통일된 규정을 제정하고, 그 규정을 모법으로 하여 각 연구기관이 내부 규정을 만들도록 유도해야 함
3. 2002년 2월에 김 홍신 전의원이 보건복지 위원회에서 발의한 실험동물 법안에 실험동물의 복지에 관한 내용이 잘 기술되어 있음.
4. 향후 실험동물 복지에 관한 규정의 제정과, 구체적인 운영 위원회의 구 성 등이 빠른 속도로 진행될 것으로 기대함
< 3R 운동 3R 운동 (Russell과 Burch) >
1. 동물 수의 감소 (Reduction) 2. 실험동물의 대체 (Replacement) 3. 동물실험의 세련화 (Refinement)
<3R 운동의 적용>
1. 동물 수의 감소 (Reduction) - 불필요한 동물실험을 재검토 (LD50 수의 감소)
2. 실험동물의 대체 (Replacement) - 하등동물, 배양세포, 컴퓨터시뮬레이션 사용
3. 동물실험의 세련화 (Refinement) - 동물의 반응을 안정화 (동물품질 향상, 사육환경 정비) - 실험결과의 호환성 (실험기법의 표준화) - 실험동물에게 주는 고통의 경감
< 동물실험의 대체방법 (Replacement) >
․동물실험의 대체방법의 충분한 검색 및 고려 ․
동일한 실험물질에 대하여 실험한 정보의 중복여부의 검색 동물실험의 감소 (Reduction) ․
연구목적과 실험 설계된 동물 수의 일치성 ․
정확한 통계학적 분석을 통한 합리적인 실험군 크기 선택 ․
실험모델 선정의 적합성(동물계통 및 종류) 동물실험의 개량(Refinement) ․
실험동물의 고통과 스트레스에 대한 평가의 적절성 ․
환경 엔리치먼트(Enrichment) 고려 여부 ․
고통경감을 위한 진정․진통․마취제 사용 고려여부 ․
인도적 종료시점(Humane endpoint)의 적절성
'스터디 > 면접대비' 카테고리의 다른 글
| 튜바리우스(tubarius) 샘 (0) | 2020.10.25 |
|---|---|
| (면접) 지질대사 질병 (0) | 2020.09.04 |
| 경계자 (면접) (0) | 2020.09.02 |
| 생물의 정의, 생식(기초) (0) | 2020.09.02 |
| 생물체의 다양성 (0) | 2020.09.02 |


